2019下半年初中化學教師資格證面試真題及答案第三批
一、考題回顧
題目:《結晶》

3基本要求:
(1)要求學生能夠進行相關的操作。
(2)要有適當的板書設計。
(3)試講要條理清晰,重點突出。
(4)教學過程中注意對學生進行啟發、引導。
注:圖片節選自上海教育出版社初中化學九年級下冊第21頁
二、考題解析
環節一:導入新課
【多媒體展示】海水曬鹽場。
【提出問題】海水曬鹽的原理是怎樣的?用自己的語言進行說明。
【學生回答】海水中含有氯化鈉,在曬鹽的過程中,水分蒸發但是氯化鈉不會蒸發,最后水分蒸發完了之后就會得到氯化鈉,實現海水曬鹽的目的。
【提出問題】從水溶液中獲取固體的方式還有哪些?如何在實驗室中實現蒸發溶劑得到固體的目的?
一起學習“蒸發與結晶”。
環節二:新課教學
1.結晶的方式
【提出問題】進行以下實驗,并分析實驗現象。說明從溶液中獲取溶質的晶體有哪些方式?
【教師實驗】
實驗1:取10 mL濃的氯化鈉溶液,用酒精燈加熱,用玻璃棒攪拌至出現較多晶體時停止加熱。
實驗2:在一個盛有30 mL沸水的燒杯中不斷加入硝酸鉀,配制成硝酸鉀飽和溶液,將燒杯放在冷水中降溫,觀察實驗現象。
【學生回答】
實驗1:有較多的晶體析出,說明通過加熱蒸發溶劑的方式可以從溶液中獲取晶體;
實驗2:放入水中降溫的燒杯中有晶體析出,說明通過給飽和溶液降溫也可以從溶液中獲取晶體。
【教師總結】在一定條件下,固體物質可以從它的水溶液中析出。人們通常把從洛液中析出晶體的過程稱為結晶。
【提出問題】從實驗中可以看出,結晶的方式有哪些?
【學生回答】蒸發溶劑結晶,降溫結晶。
【教師總結】將溶液加熱蒸發,使溶液達到飽和后,再蒸發掉溶劑,溶質就會結晶析出,比如氯化鈉的水溶液。對溶解度受溫度變化影響較大的固態物質,比如硝酸鉀等,還可以用冷卻熱的飽和溶液的方法,使溶質從溶液中結晶析出。這也就是從溶液中獲取晶體的兩種方式:蒸發結晶與冷卻結晶。
2.蒸發結晶
【提出問題】在實驗室中,要通過蒸發結晶的方式得到晶體,正確的操作是怎樣的?結合剛才教師的操作進行說明。
【學生回答,教師總結】
①蒸發皿中的液體量不宜超過蒸發皿容積的2/3;
②加熱時,應不斷用玻璃棒攪拌溶液,防止液體因局部溫度過高造成液滴飛濺;
③加熱到蒸發皿中出現較多量固體時,停止加熱,并用玻璃棒不斷攪拌,利用余熱將濾液蒸干;
④熱的蒸發皿應用坩堝鉗夾持小心地放在石棉網上。
【教師引導】參照實驗操作要領完成食鹽水的蒸發結晶操作。
(學生實驗,教師引導。)
環節三:拓展提高
【提出問題】生活在鹽湖附近的人們習慣“冬天撈堿,夏天曬鹽”,請說明其中所蘊含的分別是通過何種方式結晶?
【解析】“夏天曬鹽”是因為食鹽的溶解度受溫度變化的影響不大,夏天氣溫高,水分蒸發快,食鹽易結晶析出;“冬天撈堿”是因為純堿的溶解度受溫度變化的影響較大,冬天氣溫低,純堿易結晶析出。因此“夏天曬鹽”蘊含的是蒸發結晶,“冬天撈堿”蘊含的是降溫結晶。
根據溶解度受影響的大小,選擇結晶的操作方法——蒸發結晶或降溫結晶法;溶解度受溫度影響不大的物質結晶時一般采取蒸發結晶的方法,溶解度受溫度影響較大的物質結晶時一般采取降溫結晶的方法。
環節四:小結作業
小結:學生總結本節課重點知識,教師補充。
作業:課下思考——混有少量氯化鈉晶體的硝酸鉀,如何應用本節課的知識提純硝酸鉀?
……………………………………………………………………
一、考題回顧
題目:《鐵的冶煉》
3.基本要求:
(1)要有適當的板書設計。
(2)試講要條理清晰,重點突出。
(3)教學過程中注意對學生進行啟發、引導。
注:圖片節選自人民教育出版社初中化學九年級下冊第16頁
二、考題解析
【教學過程】
環節一:情境導入
【媒體播放】自然界中存在的金屬單質:金、銀。
【教師總結】根據之前所學的金屬活動性順序判斷,金、銀這些金屬都不活潑,在自然界中能夠以單質形式存在。那么對于鈉、鎂、鐵、銅這些相對來說活潑一些的金屬呢,在自然界中是否存在它們的單質。
【學生回答】不存在。因為:①化學性質活潑,易與其他物質發生反應;②主要以化合物的形式存在于金屬礦石中。
【媒體播放】一些鐵礦石、銅礦石的圖片。
【提出問題】在金屬活動性順序表中靠前位置的金屬性質活潑,經地殼變化不可能存在單質,多以化合物形式存在于礦石中,如何獲取日常需要的金屬單質?
【學生回答】冶煉金屬。
【提出問題】人類對地球上金屬礦物資源的利用主要是冶煉金屬,其中冶煉量最大的金屬是哪一種,請學生根據自己的生活實際來進行回答。
【學生回答】鐵!
【教師引導】那龔曄當中是如何大量的冶煉金屬鐵的,這節課共同來學習。
環節二:探究新知
【教師引導】如何把鐵單質從鐵礦石中還原出來呢?
1.鐵的冶煉
【視頻播放】我國冶煉鐵的歷史。
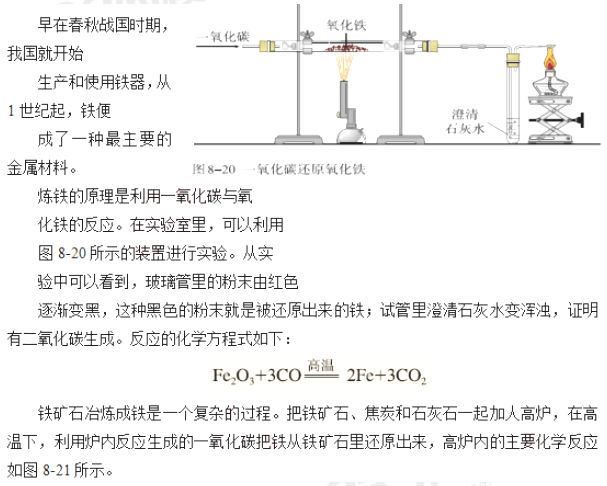
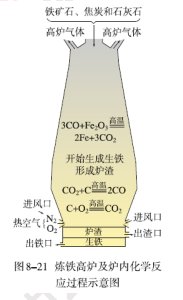
【提出問題】古人采用生熟煉鐵爐來冶煉鐵,那么當代冶煉鐵的原理是什么呢?請學生閱讀教材回答,并書寫化學方程式。
…………………………………………………………
一、考題回顧
題目:《溶質的質量分數》

二、考題解析
【教學過程】
環節一:生活導入
【教師展示】教師課堂上展示三杯顏色深淺不一的紅糖水。
【教師提問】猜想三杯紅糖水的甜度大小?判斷的依據是什么?并請學生上臺品嘗驗證。
【學生回答】根據紅糖水的顏色判斷,顏色深的甜度大,顏色淺的甜度低。
【教師提問】為什么可以通過顏色的深淺判斷溶液的濃稀?
【學生回答】顏色越深,說明溶解的紅糖越多,所以紅糖水越甜。
【教師提問】根據溶液深淺可以粗略判斷溶液的稀濃,實際生產生活中往往需要準確知道一個溶液里溶質的含量。比如,施用農藥時需要準確知道一定量的藥液里所含農藥的量。這是為什么?
【學生回答】藥液過濃,會毒害農作物;藥液過稀,則不能有效地殺蟲滅菌,因此需要準確知道溶液的組成。
【教師引導】如何定量地表示溶液的稀濃?
環節二:探究新知
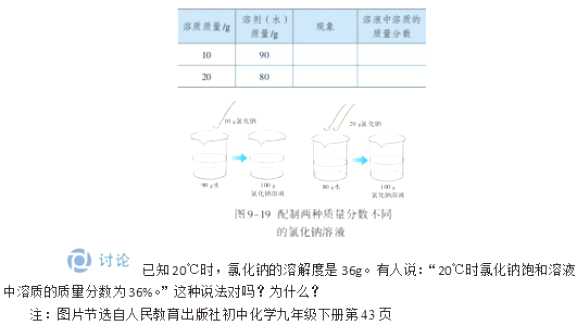
【教師演示】在室溫下,對三個小燒杯進行編號,各加入20ml水,然后分別加入0.1g、0.5g、2g無水硫酸銅,振蕩,使硫酸銅全部溶解,比較三種硫酸銅溶液的顏色,并填入表格中。
【提出問題】請同學們判斷三種硫酸銅溶液的稀濃,并解釋原因。
【學生回答】1號燒杯溶解的硫酸銅最少,顏色最淺,溶液最稀;3號燒杯溶解的硫酸銅最多,顏色最深,溶液最濃。
【教師提問】在本實驗中,溶質、溶劑和溶液分別是什么?請同學們將表格相應部分補充完整。
【學生回答】溶質是硫酸銅,溶劑是水,硫酸銅溶質分散到溶劑水中形成均一、穩定的硫酸銅溶液。
【教師提問】三種硫酸銅溶液有什么不同?從中可以得到什么信息?
【學生回答】由實驗可以看出,三種硫酸銅溶液含有不同質量的硫酸銅,所形成的溶液顏色也不同。可以得出,在一定質量的溶劑中,溶質質量不同,可以得到具有不同組成的硫酸銅溶液。
【教師引導】利用溶質質量與溶液質量的關系可以準確定量地表示溶液的組成,即溶質的質量分數。


真題推薦:歷年教師資格證面試真題>>>
教師資格證面試如何快速通關?233網校還原面試情景現場,助你一舉攻下“結構化面試+試講+答辯”三大內容,實戰通關!試聽課程>>
答疑解惑:添加小編微信個人號【ks233wx3】,或關注微信公眾號【jiaoshi_233】搜索微信公眾號“233網校教師資格證考試”,關注即可一對一答疑解惑!

